Erreurs médicamenteuses
Les acteurs mobilisés autour du signalement
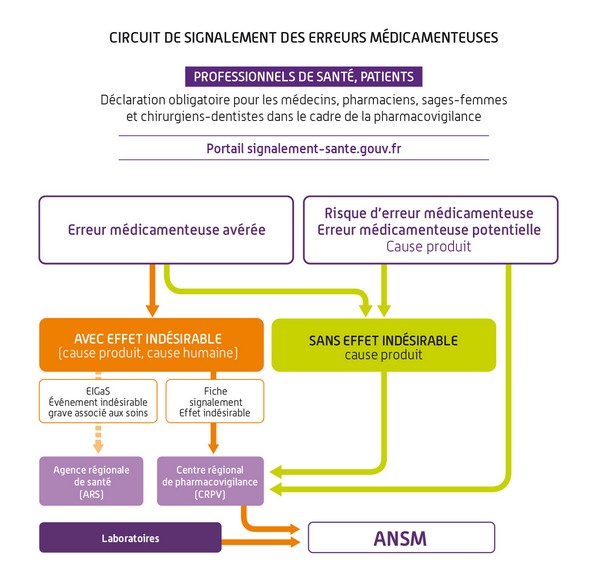
Depuis 2005, l’ANSM organise avec les Centres régionaux de Pharmacovigilance, le recueil et le traitement des signalements au sein du "Guichet Erreurs Médicamenteuses".
Les signalements pris en charge par l'ANSM mettent en cause le médicament en lui-même, et peuvent notamment concerner :
- sa dénomination : dénomination commerciale ou dénomination commune internationale (ex : risque de confusion par similitude entre deux noms de spécialités)
-
sa présentation
:
- le conditionnement (ex : défaut de conditionnement et inadaptation aux pratiques)
- l’étiquetage (ex : similitudes d’étiquetage entre deux spécialités)
- l’information (ex : informations manquantes, mentions)
|
Les signalements d'erreur mettant en cause l'organisation des soins ne rentrent pas dans le champs d'activité de l'ANSM. |
L’Agence évalue et analyse chaque signalement. Elle peut mettre en place des mesures pour que l’erreur ne se reproduise pas :
- des actions concrètes et immédiates sur le produit (modification de son conditionnement, correction de la notice…),
- des alertes auprès des professionnels ou du grand public,
- ou des recommandations de bonnes pratiques d’ordre plus général
|
En savoir plus sur le cadre réglementaire
-
Décret du 12 novembre 2010
:
propose comme définition d’un évènement indésirable associé aux soins "tout incident
préjudiciable à un patient hospitalisé survenu lors de la réalisation d'un acte de prévention, d'une investigation ou d'un traitement" -
Décret d’application du 8 novembre 2012
(Transposition de la directive
2010/84/EU ) : renforcement des dispositions en matière de sécurité des médicaments à usage humain soumis à autorisation de mise sur le marché et à la pharmacovigilance ajoute au champ de la pharmacovigilance les signalements de surdosage, de mésusage, d'abus et d'erreur médicamenteuse. - Arrêté du 6 avril 2011 : management de la qualité de la prise en charge médicamenteuse et aux médicamenteux dans les établissements de santé définie l’erreur médicamenteuse comme une « omission ou une réalisation non intentionnelle d’un acte au cours du processus de soins impliquant un médicament, qui peut être à l’origine d’un risque ou d’un évènement indésirable pour le patient "
- CIRCULAIRE N°DGOS N° DGOS/PF2/2012/72 du 14 février 2012
(28/11/2018)
 (511 ko) : Management de la qualité de la prise en charge médicamenteuse dans les établissements de santé - Actions prioritaires: liste des 12 « never events » : Evénements "qui ne devraient jamais arriver" en établissement de santé dans le cadre de la prise en charge médicamenteuse
(511 ko) : Management de la qualité de la prise en charge médicamenteuse dans les établissements de santé - Actions prioritaires: liste des 12 « never events » : Evénements "qui ne devraient jamais arriver" en établissement de santé dans le cadre de la prise en charge médicamenteuse

2008 - Copyrights AFSSAPS




 Assurer les vigilances
Assurer les vigilances


