




Lutényl/Lutéran
Questions/Réponses sur le risque de méningiome sous Lutényl/Lutéran et leurs génériques
En juin 2020 une vaste étude épidémiologique a permis de quantifier pour la première fois le risque de méningiome associé à l’utilisation d’acétate de nomégestrol (Lutényl et génériques) et d’acétate de chlormadinone (Lutéran et génériques) dès lors que leur utilisation est prolongée et à dose élevée :
- une femme qui prend l’un de ces traitements pendant plus de six mois a environ 3,3 fois plus de risque de développer un méningiome par rapport au risque de base
- le risque augmente avec la durée du traitement, la dose utilisée et l’âge de la patiente :
- sous Lutényl le risque est multiplié par 12,5 à partir de cinq ans de traitement
- sous Lutéran, il est multiplié par 7 pour 3,5 ans de traitement
Compte tenu de ces nouvelles données, nous avons mis en place un comité d’experts chargé d’établir les conditions appropriées d’utilisation et de suivi du traitement par Lutényl et Lutéran.
Ces recommandations sont consultables ICI.
- Dans quelles situations l'acétate de nomégestrol (Lutényl) et l’acétate de chlormadinone (Lutéran) peuvent désormais être utilisés? Quelles sont les nouvelles recommandations?
- Qu’est-ce qu’un méningiome ?
- Quels sont les symptômes d’un méningiome ?
- Puisque Lutényl, Lutéran et leurs génériques augmentent le risque de méningiome, pourquoi ne sont-ils pas retirés du marché ?
- Je suis traitée actuellement par Lutényl, Lutéran ou leurs génériques, que dois-je faire ?
- Quels sont les risques à arrêter moi-même mon traitement ?
- Si mon médecin me prescrit une IRM, est-ce que je dois la passer en urgence ?
- Je suis ou j’ai été sous Lutényl, Lutéran ou leurs génériques et un méningiome m’a été détecté. Vais-je devoir me faire opérer ?
- Est ce que d'autres médicaments progestatifs peuvent être concernés par le risque de méningiome?
- Est-ce que le risque de méningiome lié à ces médicaments est un risque connu ?
- Les professionnels de santé ont-ils été informés? Quelles recommandations leur ont été données ?
- Je suis professionnel de santé et je traite des femmes avec Lutényl, Lutéran ou leurs génériques, que dois-je faire ?
- Comment est-ce que je peux déclarer un effet indésirable lié à mon traitement par Lutényl, Lutéran ou leurs génériques?
1 / Dans quelles situations l’acétate de nomégestrol (Lutényl) et l’acétate de chlormadinone (Lutéran) peuvent désormais être utilisés ? Quelles sont les nouvelles recommandations d’utilisation ?
Des utilisations en dehors des indications approuvées ont également été rapportées : Lutényl et Lutéran ont pu par exemple être prescrits en tant que pilule contraceptive ou comme traitement de l’acné.
Compte-tenu du sur-risque démontré de méningiome associé à la prise d’acétate de nomégestrol (Lutényl et génériques) et d’acétate de chlormadinone (Lutéran et génériques), voici nos recommandations d’utilisation :
Version téléchargeable (21/01/2021)  (158 ko)
(158 ko)
Ces recommandations se basent sur les réflexions menées par le comité d’experts composé de médecins et d’acteurs associatifs qui a été mis en place pour définir les conditions de prise en charge par ces traitements, au regard du risque de méningiome.
Cliquer ICI pour consulter les recommandations complètes
2 / Qu’est-ce qu’un méningiome ?
Le méningiome est une tumeur qui se développe à partir des méninges (enveloppes autour du cerveau). Ces tumeurs sont le plus souvent non cancéreuses mais peuvent être à l'origine de troubles graves pouvant nécessiter une intervention chirurgicale lourde et à risque.
Dans la population générale, on observe chaque année environ 9 à 10 nouveaux cas de méningiome pour 100 000 patients.
3 / Quels sont les symptômes d’un méningiome ?
Les signes peuvent être très différents selon la taille et la localisation de la tumeur.
Les symptômes les plus souvent rencontrés sont : maux de tête fréquents, vertiges, troubles de la vision, faiblesse dans les bras ou les jambes, paralysie, troubles du langage ou de l’audition, troubles de l’odorat, convulsions, troubles de la mémoire.
Si vous êtes ou que vous avez été traitée par Lutényl, Lutéran ou leurs génériques et que vous présentez un ou plusieurs de ces symptômes, consultez votre médecin qui vous prescrira une IRM cérébrale de contrôle.
En cas de doute n’hésitez pas à vous adresser à votre médecin.
4 / Puisque Lutényl, Lutéran et leurs génériques augmentent le risque de méningiome, pourquoi ne sont-ils pas retirés du marché ?
Ces médicaments sont utiles pour prendre en charge certaines pathologies pouvant avoir un retentissement sur la qualité de vie des patientes (notamment pour les femmes souffrant d’endométriose ou de fibromes utérins).
Compte tenu de l’intérêt thérapeutique que présentent ces médicaments, leur commercialisation en France n’est pas remise en cause.
5 / Je suis traitée actuellement par Lutényl, Lutéran ou leurs génériques, que dois-je faire ?
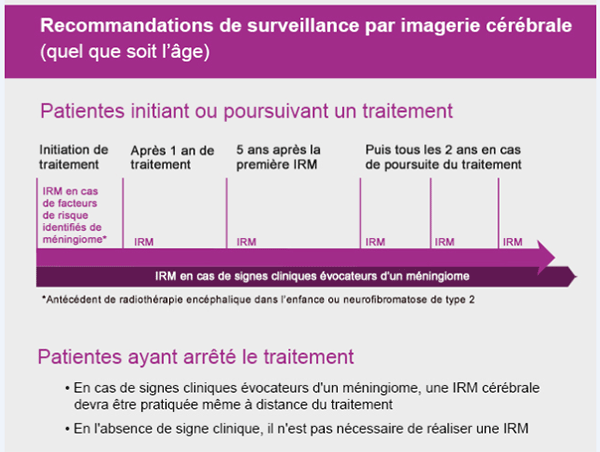
Quel que soit votre âge, vous devez réaliser un examen par imagerie cérébrale (IRM) dans les situations suivantes :
- à tout moment pendant ou après votre traitement en cas de symptômes ou de signes évocateurs d’un méningiome ;
- au bout d’1 an de traitement si votre traitement nécessite d’être poursuivi, puis 5 ans après la première IRM, puis tous les 2 ans tant que votre traitement est poursuivi ;
- à l'initiation du traitement si vous présentez des facteurs de risque de méningiome (antécédent de radiothérapie encéphalique dans l’enfance ou neurofibromatose de type 2).
Si un méningiome est diagnostiqué pendant votre traitement, vous devez arrêter de prendre votre médicament. Votre médecin devra aussi vous orienter vers une consultation de neurochirurgie afin d’évaluer si une intervention chirurgicale est nécessaire ou non.
6 / Quels sont les risques à arrêter moi-même mon traitement ?
Si vous êtes actuellement traitée par Lutényl, Lutéran, ou leurs génériques nous vous invitons à consulter votre médecin (traitant ou gynécologue) pour discuter avec lui de votre prise en charge. Il est en effet le mieux à même de juger de la pertinence de votre traitement en tenant compte de votre situation médicale personnelle dans son ensemble (= bénéfice / risque individuel).
C’est à cette occasion que sera prise la décision d’arrêter ou de poursuivre votre traitement.
Si vous souhaitez arrêter votre traitement il est préférable d’en parler avec votre médecin avant de prendre votre décision.
A priori, il n’existe pas de risque à mettre fin soi-même à son traitement. Néanmoins, pour certaines utilisations comme l’endométriose ou les fibromes utérins, l’arrêt du traitement peut être associé à la réapparition de certains symptômes (notamment saignements et douleurs).
Ces médicaments ayant un effet contraceptif, si vous décidez d’arrêter votre traitement, votre contraception ne sera plus assurée et il vous faudra envisager une nouvelle méthode contraceptive.
7 / Si mon médecin me prescrit une IRM, est-ce que je dois la passer en urgence ?
Si votre médecin vous a prescrit une IRM cérébrale à la suite de signes évocateurs d’un méningiome (maux de tête fréquents, vertiges, troubles de la vision, faiblesse dans les bras ou les jambes, paralysie, troubles du langage ou de l’audition, troubles de l’odorat, convulsions, troubles de la mémoire,…), nous vous invitons à faire réaliser cette IRM dès que possible.
En l’absence de symptôme neurologique, si votre médecin vous a prescrit une IRM de contrôle dans le cadre d’une prise de traitement depuis plus de 5 ans, elle pourra être réalisée sans urgence.
8 / Je suis ou j’ai été traitée par Lutényl, Lutéran ou leurs génériques et un méningiome m’a été détecté. Vais-je devoir me faire opérer ?
Si un méningiome est détecté alors que vous êtes traitée par Lutényl, Lutéran ou leurs génériques, votre médecin vous demandera d’arrêter votre traitement et vous ne devrez jamais reprendre ces médicaments, ni même de l’acétate de cyprotérone (Androcur et génériques) ; on dit que ces médicaments sont contre-indiqués en cas de méningiomes ou d’antécédent de méningiome.
Votre médecin devra aussi vous orienter vers une consultation de neurochirurgie afin d’évaluer si une intervention chirurgicale est nécessaire ou non.
9 / Est-ce que d’autres médicaments progestatifs peuvent être concernés par le risque de méningiome ?
Une première étude de pharmaco-épidémiologie conduite en 2018 par le groupement d’intérêt scientifique Epi-Phare sur l’acétate de cyprotérone (Androcur et génériques) a mis en évidence le risque de méningiome lié à l’utilisation de ce médicament.
Une autre étude a ensuite été conduite par Epi-Phare sur deux autres traitements progestatifs qui avaient également fait l’objet de signalements de cas de méningiome. Ces deux progestatifs sont l’acétate de nomégestrol (Lutényl et génériques) et l’acétate de chlormadinone (Lutéran et génériques).
Cette étude confirme le sur-risque de développer un méningiome lié à l’utilisation du Lutényl et Lutéran (et leurs génériques).
| Acétate de nomegestrol (Lutényl et génériques) | Acétate de chlormadinone (Lutéran et génériques) | Acétate de cyprotérone 50 mg (Androcur et génériques) |
|
| Multiplication du risque de méningiome par rapport au risque de base | x 3,3 au-delà de 6 mois d’utilisation |
x 3,4 au-delà de 6 mois d’utilisation |
x 7 au-delà de 6 mois de traitement |
| x 12,5 à partir d’une dose cumulée correspondant à 5 ans de traitement (5 mg /20 jours par mois) |
x 7 à partir d’une dose cumulée correspondant à 3,5 ans d’utilisation (10 mg /20 jours par mois) |
x 20 à partir de 5 ans de traitement |
Par ailleurs, l’ANSM surveille étroitement l’ensemble des cas rapportés de méningiomes sous progestatifs. A cet égard, le deuxième volet de l’enquête de pharmacovigilance en cours depuis octobre 2018 sera présenté en fin d’année 2020 lors d’un Comité scientifique permanent (CSP) surveillance et pharmacovigilance.
10 / Est-ce que le risque de méningiome lié à ces médicaments est un risque connu ?
En février 2019, à la suite de signalements de cas de méningiome une lettre a été adressée aux professionnels de santé afin de les informer du risque potentiel de méningiome sous acétate de nomegestrol (Lutényl et génériques) ou acétate de chlormadinone (Lutéran et génériques).
Cette lettre de février 2019 consultable ICI .
Les résultats d’une vaste étude épidémiologique récente (étude du GIS Epi-Phare de juin 2020) permettent pour la première fois de quantifier ce risque : il augmente avec la durée du traitement, la dose utilisée et l’âge de la patiente.
Globalement, à partir de 6 mois d’utilisation de Lutényl, Lutéran ou un générique, le risque de développer un méningiome est multiplié par plus de 3.
Sous Lutényl, à partir de 5 ans de traitement le risque est multiplié par 12,5.
Sous Lutéran à partir de 3,5 ans de traitement le risque est multiplié par 7.
| Acétate de nomégestrol (Lutényl et génériques) | Acétate de chlormadinone (Lutéran et génériques) | |
| Multiplication du risque de méningiome par rapport au risque de base | x 3,3 au-delà de 6 mois d’utilisation | x 3,4 au-delà de 6 mois d’utilisation |
| x 12,5 à partir d’une dose cumulée correspondant à 5 ans de traitement (5 mg /20 jours par mois) |
x 7 à partir d’une dose cumulée correspondant à 3,5 ans d’utilisation (10 mg /20 jours par mois) |
Par ailleurs le risque de méningiome conduisant à une intervention chirurgicale au niveau du crâne (= chirurgie intracrânienne) augmente fortement avec l’âge : il est, par exemple, 3 fois plus élevé pour les femmes âgées de 35 à 44 ans que pour celles âgées de 25 à 34 ans.
11 / Les professionnels de santé ont-ils été informés ? Quelles recommandations leur ont été données ?
Les recommandations de janvier 2021 ont été adressées aux professionnels de santé concernés (endocrinologues, gynécologues, neurochirurgiens, neurologues, médecins généralistes, radiologues, et pharmaciens d’officine et hospitaliers).
En octobre 2020, un message reprenant les principaux éléments chiffrés portant sur le sur-risque de méningiome a également été envoyé à ces professionnels de santé.
En février 2019, ils ont reçu un premier courrier d’information faisant état des données de pharmacovigilance disponibles à ce moment-là.
12 / Je suis professionnel de santé et je traite des femmes avec Lutényl, Lutéran ou leurs génériques, que dois-je faire ?
Nous vous invitons à faire le point avec votre patiente, notamment concernant la pertinence de maintenir son traitement et la nécessité de réaliser un suivi par IRM.
Nos recommandations sont les suivantes :
Situations pour lesquelles l’utilisation de Lutényl/Lutéran peut être envisagée ou non au regard du rapport bénéfice-risque, et conduite à tenir
Télécharger les recomandations d'utilisation
(21/01/2021)  (158 ko)
(158 ko)
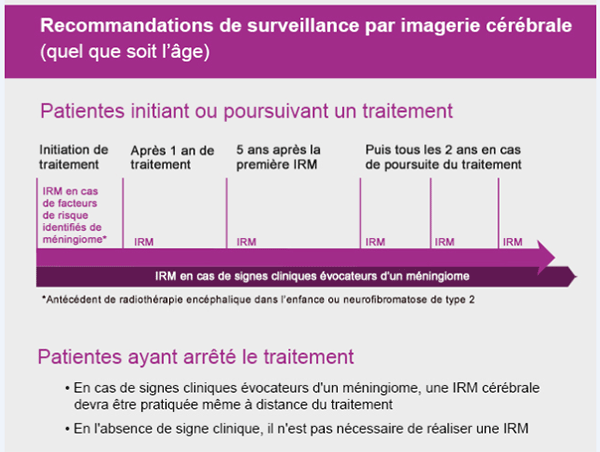
Un examen par imagerie cérébrale (IRM) doit être réalisé quel que soit l'âge de la patiente :
- à tout moment pendant ou après le traitement en cas de symptôme ou signes évocateurs d’un méningiome ;
- au bout d’1 an de traitement lorsque le traitement nécessite d’être poursuivi, puis 5 ans après la première IRM, puis tous les 2 ans tant que le traitement est poursuivi ;
- à l'initiation du traitement en cas de facteurs de risque identifiés de méningiome (antécédent de radiothérapie encéphalique dans l’enfance ou neurofibromatose de type 2).
Si la mise en place d’un traitement hormonal est envisagée ou lorsqu’une grossesse est souhaitée par la patiente, et en cas d’antécédents de méningiome (opéré ou non) en lien avec la prise d’acétate de nomégestrol, de chlormadinone ou de cyprotérone, une prise en charge pluridisciplinaire doit être mise en place.
Par ailleurs nous rappelons que :
- l’acétate de nomégestrol, l’acétate de chlormadinone et l’acétate de cyprotérone (Androcur et génériques) sont contre-indiqués en cas de méningiomes ou d’antécédent de méningiome ;
- toute identification d’un méningiome en cours d’utilisation de l’un de ces médicaments doit conduire à interrompre le traitement. Aucune de ces 3 substances ne pourra être reprise en cas de méningiome.
13 / Comment est-ce que je peux déclarer un effet indésirable lié à mon traitement par Lutényl, Lutéran ou leurs génériques?
Si vous pensez avoir développé un effet indésirable en lien avec votre traitement, nous vous invitons à le signaler directement sur le portail de signalement des évènements indésirables : signalement-sante.gouv.fr
Le signalement peut être déclaré en quelques clics directement par un le patient, par son médecin ou tout autre professionnel de santé ou encore par une association de patients ou d’usagers.
Déclarer des effets indésirables est toujours utile, cela contribue à une meilleure prise en compte des risques associés aux médicaments






