Préparations hospitalières, magistrales et officinales
Les préparations hospitalières
 |
L'essentiel sur les préparations hospitalières |
| Les préparations hospitalières (PH) sont des médicaments. Elles sont : Réalisées
Dispensées
Elaborées en conformité avec des référentiels scientifiques et de bonnes pratiques
|
|
Quelles matières premières pour réaliser des préparations hospitalières ?
Mises en garde de l’ANSM sur certaines préparations hospitalières
Acide borique |
|
Acide osmique |
|
Carmustine |
|
3.4 Diaminopyridine |
|
Hydrate de chloral |
|
Mélatonine |
|
Vitamine D |
Conformité avec les référentiels
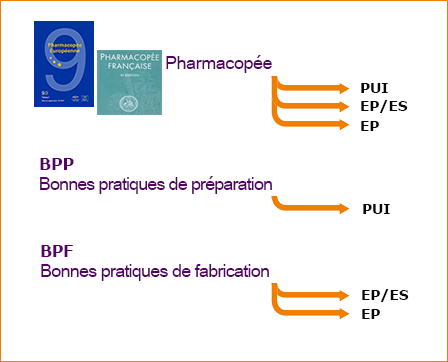 |
Les préparations hospitalières doivent être réalisées en conformité avec
|
| Pharmacopée et Formulaire national
Les préparations hospitalières sont réalisées suivant les textes généraux et les monographies de la Pharmacopée. La Pharmacopée comprend les textes de la Pharmacopée européenne et ceux de la Pharmacopée française. |
|
| Les Pharmacies à usage intérieur (PUI) doivent réaliser les préparations hospitalières en conformité avec les Bonnes pratiques de préparation (BPP) Les établissements pharmaceutiques gérés par des établissements publics de santé (EP/ES) et les établissements pharmaceutiques (EP) autorisés à fabriquer des médicaments, doivent réaliser les préparations hospitalières en conformité avec les Bonnes pratiques de fabrication (BPF) de médicaments à usage humain. |
|
L'étiquetage des préparations hospitalières
Les préparations hospitalières doivent étiquetées. (décret n°2012-1201)
Pour assurer au mieux la sécurité et la traçabilité des préparations, l’ANSM publie des recommandations et propose des modèles d’étiquettes adaptés à chaque type de situations.
Lire aussi
- Liste des Excipients à Effet Notoire - Site EMA
Sous-traitance des préparations hospitalières
La sous-traitance des préparations hospitalières consiste en l’exécution par un tiers (prestataire) de la totalité des opérations de préparation (y compris le conditionnement primaire), pour le compte d’un donneur d’ordre.
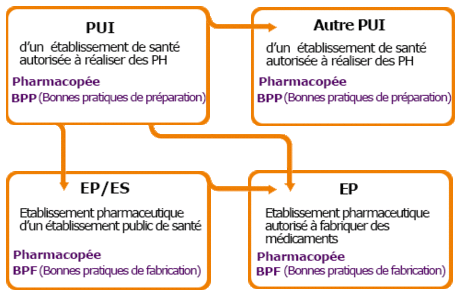 Donneur d'ordre> sous-traitance autorisée |
La sous-traitance est exécutée dans le cadre d’un contrat rédigé selon les bonnes pratiques entre le donneur d’ordre et le sous-traitant. |
Déclaration des préparations hospitalières
|
|
| Les opérateurs qui réalisent des PH sont tenus d'en déclarer la réalisation à l'ANSM. Celle -ci s'assure que les préparations sont justifiées. | |
|
|
Les préparations nouvelles ou modifiées |
Les préparations nouvelles ou modifiées doivent être déclarées dans un délai d’un mois après leur réalisation :
Quelles informations déclarer ?
|
L'arrêt de réalisation d'une PH |
L’arrêt de réalisation d’une PH doit être déclaré :
|
Le bilan qualitatif et quantitatif des PH réalisées ou cessées |
Les déclarants doivent effectuer tous les deux ans un bilan qualitatif et quantitatif des préparations réalisées ou cessées.
Le bilan qualitatif couvre la période du 1er janvier de l’année n-1 au 31 décembre de l’année n. |
|
|
| L'application informatique sécurisée PrHosper permet de :
Pour faciliter la déclaration l’application PrHosper met également à disposition des utilisateurs :
|
|
Déclaration d'effet indésirable lié à l'utilisation d'une préparation hospitalière
Tout effet indésirable (réaction nocive et non voulue) lié à l'utilisation de préparations hospitalières doit être déclaré au système national de pharmacovigilance.
Les règles de déclaration des effets indésirables communes à l’ensemble des médicaments s'appliquent aux préparations hospitalières.
Un code spécifique est attribué par l'ANSM à chaque préparation hospitalière déclarée. Il permet d'optimiser la déclaration d'éventuels effets indésirables et notamment de relier un effet indésirable à l’administration d’une PH donnée.
La déclaration peut être effectuée par les patients, les professionnels de santé, les laboratoires pharmaceutiques .
Les modalités et fiches de déclaration des effets indésirables sont spécifiques à chaque acteur.
Consulter la rubrique : Déclarer un effet indésirable
Que fait l'ANSM pour assurer la sécurité des préparations?

L’ANSM s’assure que le recours à une PH est justifié et analyse :
-
les préparations qui ne répondent pas à un besoin thérapeutique identifié
et pourraient être remplacées par des spécialités pharmaceutiques déjà disponibles en France dans le cadre d'une autorisation de mise sur le marché (AMM) ou d'une autorisation temporaire d'utilisation (ATU).
L'ANSM demande dans ce cas aux PUI de cesser la distribution de ces PH.
- les préparations répondant à un besoin thérapeutique identifié qui sont nécessaires et sans équivalent thérapeutique. L'ANSM propose une harmonisation de formules des préparations pour améliorer et standardiser leur réalisation et leur contrôle dans le respect d’une qualité optimale. Une formule est élaborée puis publiée dans la Pharmacopée française. Le pharmacien est alors tenu de se conformer strictement à la formule décrite.
Lire aussi
- Résumé du rapport d’analyse des préparations hospitalières déclarées à l’ANSM (06/09/2010)
 (685 ko) (période janvier 2008/ janvier 2010)
(685 ko) (période janvier 2008/ janvier 2010)
L’ANSM identifie les préparations "potentiellement à risque " et évalue les effets indésirables des PH.
Elle réalise un état des lieux de l’utilisation de ces préparations à l’hôpital, et si nécessaire en ville, en menant une enquête auprès de PUI et de pharmacies d’officine.
Elle procède ensuite à une évaluation de leur toxicité, en sollicitant l’avis d’experts. Elle peut alors prendre des mesures de police sanitaire adéquates telles qu’interdictions, restrictions.
L’ANSM mène des inspections dans les établissements pharmaceutiques et les établissements pharmaceutiques au sein des établissements de santé
Les préparations saisies lors de ces inspections sont analysées par ses laboratoires. Des actions correctives sont demandées, le cas échéant.
L’ANSM contribue au suivi de la réglementation , et plus particulièrement en ce qui concerne les bonnes pratiques de préparation.
Elle pilote l'actualisation du guide de bonnes pratiques de préparation s’appliquant aux officines de pharmacies et aux pharmacies à usage intérieur publié en 2007.
Lire aussi





 Réglementer, élaborer des référentiels et inspecter
Réglementer, élaborer des référentiels et inspecter